免疫療法時代における肝細胞癌治療戦略
(近畿大学病院治療戦略)
主任教授 工藤 正俊

※以下の記事は2021年3月、2021年6月、2021年11月のインタビューに基づき作成(場所:近畿大学病院)
※各薬剤の使用にあたっては電子添文をご確認ください
はじめに
2009 年にソラフェニブ*、2017 年にレゴラフェニブ、2018 年にレンバチニブ*、2019 年にラムシルマブ、2020 年にアテゾリズマブ+ベバシズマブ併用療法*ならびにカボザンチニブが承認され、肝細胞癌領域においても多くの薬剤が使用可能となった(図①)。ファーストラインとして3 剤1-3)、セカンドラインとして3 剤4-6)、計6 剤の薬物治療をいかにSequence(逐次療法)させていくか、特にBarcelona Clinic Liver Cancer(BCLC)病期分類のIntermediate stage(BCLC-B)においては、いかにこれらの薬物治療と局所治療(手術、ラジオ波焼灼療法[RFA]、肝動脈化学塞栓療法[TACE]など)を適切に選択・施行していくかが、肝細胞癌患者の予後延長へとつながる重要なポイントと考えられる。本稿では、アテゾリズマブ+ベバシズマブ併用療法が承認された免疫療法時代において、これらの薬剤をどう使い分けていくか、その治療戦略をご紹介させていただく。
*効能・効果:切除不能な肝細胞癌
図①本邦における肝細胞癌に対する薬物治療の変遷

4) Bruix J, et al.: Lancet. 2017; 389(10064): 56-66
5) Zhu AX, et al.: Lancet Oncol. 2019; 20(2): 282-296
4. 効能又は効果(一部抜粋)〈レンビマカプセル4mg〉
切除不能な肝細胞癌
5. 効能又は効果に関連する注意(一部抜粋)〈切除不能な肝細胞癌〉
5.3 局所療法(経皮的エタノール注入療法、ラジオ波焼灼療法、マイクロ波凝固療法、肝動脈塞栓療法/肝動脈化学塞栓療法、放射線療法等)の適応となる肝細胞癌患者に対する本剤の有効性及び安全性は確立していない。
Intermediate stage(BCLC-B)
Intermediate stageの治療方針は薬物治療と局所治療の適切な選択・施行により根治を目指すことであり、奏効率が高く・奏効までの期間が短い薬剤を選択する
先に述べた薬物治療の6剤における各Phase Ⅲ試験は、いずれも患者背景としてはAdvanced stage(BCLC-C)が主な対象となっている1-6)。一方で、Intermediate stage(BCLC-B)においては、これまでTACEが標準治療となっていたが、2019年にアジアから、2020年には本邦から、TACE不適の概念が専門家のコンセンサスとして提唱された7, 8)。TACE不適の病態に対しては、薬物治療としてレンバチニブを先行導入し、その後にTACEを追加するLEN-TACE Sequential療法(レンバチニブ先行投与後のTACE追加)が、「肝癌診療マニュアル 第4版」ならびに「APPLE Expert Consensus」において有効な治療法と考えられると記載されている7, 8)。
BCLC-Bでの薬物治療に求められる要素、ならびに薬物-TACE Sequential 療法の効果を最大化する上で必要となる薬物治療の要素を図②に示す。
図②薬物-TACE Sequential 療法の効果の最大化要件

10) Shimose S, et al.: Cancers (Basel). 2021; 13(1):160 KD
11) Kudo M, et al.: Gut. 2020; 69(8): 1492-1501 KD
9)の著者にエーザイ株式会社より謝金等を受領している者が含まれる。
10)の著者にエーザイ株式会社、MSD株式会社より謝金等を受領している者が含まれる。
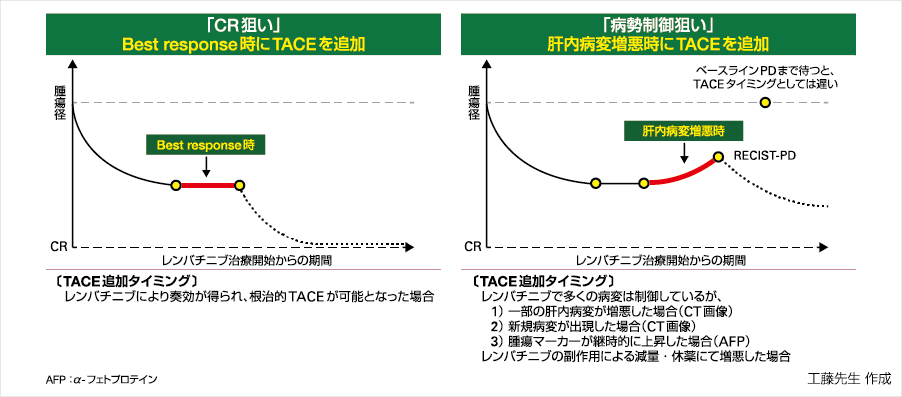
また、BCLC-BにおいてLEN-TACE Sequential療法を実施する目的とタイミングは、「CR狙い」(Best response時にTACEを追加)と「病勢制御狙い」(肝内病変増悪時にTACEを追加)の2つのパターンが考えられる(図③)。
図③Up-to-7 out(TACE不適病態)に対するLEN-TACE Sequential 療法の目的とTACE検討タイミング(イメージ図)
4. 効能又は効果(一部抜粋)〈レンビマカプセル4mg〉
切除不能な肝細胞癌
5. 効能又は効果に関連する注意(一部抜粋)〈切除不能な肝細胞癌〉
5.3 局所療法(経皮的エタノール注入療法、ラジオ波焼灼療法、マイクロ波凝固療法、肝動脈塞栓療法/肝動脈化学塞栓療法、放射線療法等)の適応となる肝細胞癌患者に対する本剤の有効性及び安全性は確立していない。
6. 用法及び用量(一部抜粋)〈切除不能な肝細胞癌〉
通常、成人には体重にあわせてレンバチニブとして体重60 kg以上の場合は12mg、体重60kg未満の場合は8mgを1日1回、経口投与する。なお、患者の状態により適宜減量する。
7. 用法及び用量に関連する注意(一部抜粋)〈切除不能な肝細胞癌〉
7.4 副作用があらわれた場合は、症状、重症度等に応じて電子添文記載の基準を考慮して、本剤を減量、休薬又は中止すること。
TACEと分子標的治療薬の併用療法の肝癌診療ガイドラインでの位置づけ
「肝癌診療ガイドライン第5 版」では、第6 章 肝動脈(化学)塞栓療法 TA(C)E CQ36「塞栓療法と分子標的治療薬を併用するのは適切か?」において、塞栓療法と分子標的治療薬の併用は、行うことを考慮してもよい(弱い推奨)と記載され、「推奨しない」としていた第4版から推奨治療(弱い推奨)へと改訂された12) 図④)。
図④肝癌診療ガイドライン改訂で塞栓療法と分子標的治療薬の併用が推奨治療(弱い推奨)に

TACEと分子標的治療薬の併用(TACE施行時、分子標的治療薬は休薬)イメージ
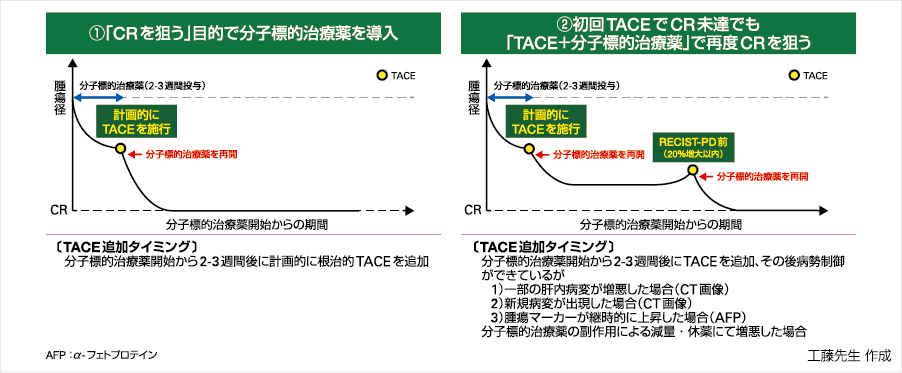
Up-to-7 in(腫瘍学的TACE 不適病態7)の場合)に対するTACEと分子標的治療薬の併用(TACE+分子標的治療薬:TACE施行時、分子標的治療薬は休薬)を前提とした治療では、①「CRを狙う」目的で分子標的治療薬を2-3 週間投与後*に根治的TACEを追加するパターンと、②同様に分子標的治療薬開始から2-3週間後*にTACEを追加し、初回はCR未達でも「TACE+分子標的治療薬」で再度CRを狙うパターンを想定することも可能である(図⑤)。
*腫瘍濃染に変化があった場合
図⑤Up-to-7 in(腫瘍学的TACE不適病態の場合)に対するTACEと分子標的治療薬の併用(TACE施行時、分子標的治療薬は休薬)を前提とした治療(イメージ図)
4. 効能又は効果(一部抜粋)〈レンビマカプセル4mg〉
切除不能な肝細胞癌
5. 効能又は効果に関連する注意(一部抜粋)〈切除不能な肝細胞癌〉
5.3 局所療法(経皮的エタノール注入療法、ラジオ波焼灼療法、マイクロ波凝固療法、肝動脈塞栓療法/肝動脈化学塞栓療法、放射線療法等)の適応となる肝細胞癌患者に対する本剤の有効性及び安全性は確立していない。
文献
1) Llovet JM, et al.: N Engl J Med. 2008; 359(4): 378-390
2) Kudo M, et al.: Lancet. 2018; 391(10126): 1163-1173[LEN-0172]
本試験はエーザイ株式会社の支援を受けて実施された。
3) Finn RS, et al.: N Engl J Med. 2020; 382(20): 1894-1905
4) Bruix J, et al.: Lancet. 2017; 389(10064): 56-66
5) Zhu AX, et al.: Lancet Oncol. 2019; 20(2): 282-296
6) Abou-Alfa GK, et al.: N Engl J Med. 2018; 379(1): 54-63
7) 日本肝臓学会 編「肝癌診療マニュアル 第4 版」2020 年, P212, 医学書院
8) Kudo M, et al.: Liver Cancer. 2020; 9(3): 245-260
9) Kawamura Y, et al.: Liver Cancer. 2020; 9(6): 756-770
10) Shimose S, et al.: Cancers (Basel). 2021; 13(1):160
11) Kudo M, et al.: Gut. 2020; 69(8): 1492-1501
12) 日本肝臓学会 編「肝癌診療ガイドライン 2021 年版」2021 年, P16-18, P196-197, 金原出版
以下の著者にエーザイ株式会社、MSD 株式会社より謝金等を受領している者が含まれる。
2), 4), 5), 6),8), 11)
以下の著者にエーザイ株式会社より謝金等を受領している者が含まれる。
1), 3), 9)
